Jest nowa lista refundacyjna. Jakie zmiany zaczną obowiązywać 1 stycznia 2023 r.
Nowe obwieszczenie refundacyjne wprowadza m.in. kompleksowe zmiany w opisie programu lekowego B.54. Leczenie chorych na szpiczaka plazmocytowego, a także zmiany w programie lekowym dla chorych na przewlekłą białaczkę limfocytową oraz chorych na klasycznego chłoniaka Hodgkina.

W Dzienniku Urzędowym Ministra Zdrowia opublikowano obwieszczenie w sprawie wykazu refundowanych leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych, obowiązującego od 1 stycznia 2023 r.
Jakie zmiany w programach lekowych od 1 stycznia 2023 r.
Oto najważniejsze zmiany w programach lekowych, które zaczną obowiązywać od stycznia 2023 r.
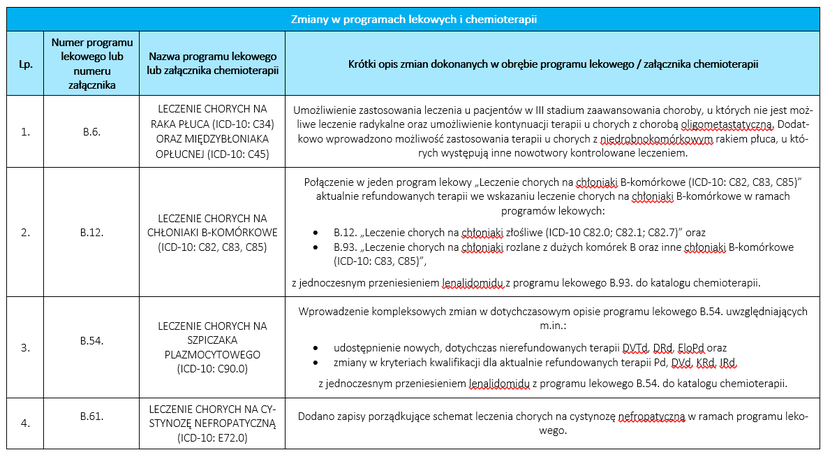
Leczenie chorych na raka płuca (ICD-10: C34) oraz międzybłoniaka opłucnej (ICD-10: C45) - umożliwienie zastosowania leczenia u pacjentów w III stadium zaawansowania choroby, u których nie jest możliwe leczenie radykalne oraz umożliwienie kontynuacji terapii u chorych z chorobą oligometastatyczną. Dodatkowo wprowadzono możliwość zastosowania terapii u chorych z niedrobnokomórkowym rakiem płuca, u których występują inne nowotwory kontrolowane leczeniem.
Połączenie w jeden program lekowy „Leczenie chorych na chłoniaki B-komórkowe (ICD-10: C82, C83, C85)” aktualnie refundowanych terapii we wskazaniu leczenie chorych na chłoniaki B-komórkowe w ramach programów lekowych:
- B.12. „Leczenie chorych na chłoniaki złośliwe (ICD-10 C82.0; C82.1; C82.7)” oraz
- B.93. „Leczenie chorych na chłoniaki rozlane z dużych komórek B oraz inne chłoniaki B-komórkowe (ICD-10: C83, C85)”,
z jednoczesnym przeniesieniem lenalidomidu z programu lekowego B.93. do katalogu chemioterapii.
Wprowadzenie kompleksowych zmian w dotychczasowym opisie programu lekowego B.54. Leczenie chorych na szpiczaka plazmocytowego, uwzględniających m.in.:
- udostępnienie nowych, dotychczas nierefundowanych terapii DVTd, DRd, EloPd oraz
- zmiany w kryteriach kwalifikacji dla aktualnie refundowanych terapii Pd, DVd, KRd, IRd,
z jednoczesnym przeniesieniem lenalidomidu z programu lekowego B.54. do katalogu chemioterapii.
Połączenie w jeden program lekowy „Leczenie chorych na klasycznego chłoniaka Hodgkina (ICD-10: C81)” aktualnie refundowanych terapii we wskazaniu leczenie chorych na chłoniaka Hodgkina w ramach progra-mów lekowych:
- B.77. „Leczenie chorych na chłoniaki CD30+ (C 81; C 84.5)” oraz
- B.100. „Leczenie chorych na oporną i nawrotową postać klasycznego chłoniaka Hodgkina z zasto-sowaniem niwolumabu (ICD-10: C81)”, z jednoczesnym:
- zniesieniem kryterium kwalifikacyjnego do leczenia brentuksymabem vedotin chorych na chłoniaka Hodgkina ze stwierdzonym nawrotem lub opornością na leczenie, tj.: „nieobecność przeciwwskazań do allogenicznego przeszczepienia komórek krwiotwórczych w razie uzyskania odpowiedzi częściowej”.
Zmiany w kryteriach kwalifikacji do leczenia niwolumabem (umożliwienie leczenia w przypadku nawrotu lub oporności na leczenie brentuksymabem vedotin, gdy auto-HSCT nie stanowiło opcji leczenia, umożliwienie leczenia pacjentów o stanie sprawności wg ECOG: 2).
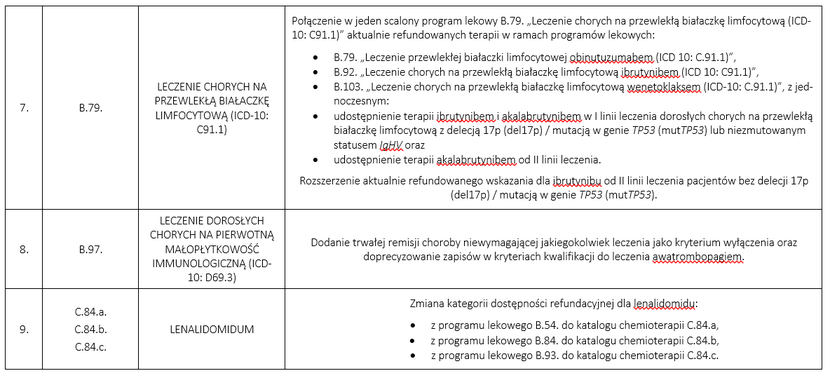
Połączenie w jeden scalony program lekowy B.79. „Leczenie chorych na przewlekłą białaczkę limfocytową (ICD-10: C91.1)” aktualnie refundowanych terapii w ramach programów lekowych:
- B.79. „Leczenie przewlekłej białaczki limfocytowej obinutuzumabem (ICD 10: C.91.1)”,
- B.92. „Leczenie chorych na przewlekłą białaczkę limfocytową ibrutynibem (ICD 10: C91.1)”,
- B.103. „Leczenie chorych na przewlekłą białaczkę limfocytową wenetoklaksem (ICD-10: C.91.1)”, z jednoczesnym:
- udostępnieniem terapii ibrutynibem i akalabrutynibem w I linii leczenia dorosłych chorych na prze-wlekłą białaczkę limfocytową z delecją 17p (del17p) / mutacją w genie TP53 (mutTP53) lub niezmu-towanym statusem IgHV oraz
- udostępnieniem terapii akalabrutynibem od II linii leczenia.
Rozszerzenie aktualnie refundowanego wskazania dla ibrutynibu od II linii leczenia pacjentów bez delecji 17p (del17p) / mutacją w genie TP53 (mutTP53).

Zmiany w refundacji aptecznej od 1 stycznia 2023 r.
W ramach wskazań pozarejestracyjnych nie będzie kontynuowana refundacja:

Po analizie zapisów ChPL wskazanie refundacyjne dla leków inhalacyjnych zawierających beklomtazon + formoterol w dawce 200+6 µg/dawkę zostało zawężone do astmy.
Lek Tresiba (insulina degludec) refundowany dotychczas w aptece we wskazaniu:
- Cukrzyca typu I u dorosłych; Cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥8% oraz cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca o znanej przyczynie (zgodnie z definicją wg WHO);
- Cukrzyca typu I u dzieci powyżej 1. roku życia i młodzieży. Cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥8% oraz cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca u dzieci powyżej 1. roku życia i młodzieży o znanej przyczynie (zgodnie z definicją wg WHO)
nie znajdzie się na kolejnym wykazie refundacyjnym obowiązującym od 1 stycznia 2023 r., ponieważ podmiot odpowiedzialny Novo Nordisk Pharma Sp. z o.o. nie spełnił ustawowego warunku wynikającego z art. 13 ust. 2 ustawy z dnia 12 maja 2011 r. o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych odnośnie konieczności obniżenia urzędowej ceny zbytu o 25% w związku z upływem okresu wyłączności rynkowej dla tego preparatu. Podmiot deklaruje jednak stałą dostępność obu prezentacji leku w aptekach ogólnodostępnych z ustaloną przez producenta ceną.
Decyzja o braku kontynuowania refundacji jest autonomiczną decyzją podmiot odpowiedzialny Novo Nordisk Pharma Sp. z o.o., a lek Tresiba będzie mógł być ponownie objęty refundacją, o ile firma złoży odpowiedni wniosek, spełniający warunki opisane w ustawie o refundacji.
Podsumowanie zmian w styczniowym obwieszczeniu refundacyjnym
- W związku z wydaniem pozytywnych decyzji o objęciu refundacją ogółem do wykazu zostało dodanych 137 produktów bądź nowych wskazań.
- Dla 99 produktów wprowadzono obniżki urzędowych cen zbytu (od 0,01 zł do 4 460,40 zł).
- Dla 32 produktów podwyższono urzędowe ceny zbytu (od 0,10 zł do 43,20 zł).
- Dla 292 pozycji w obwieszczeniu spadnie dopłata pacjenta (od 0,01 zł do 63,76 zł).
- Dla 426 pozycji w obwieszczeniu wzrośnie dopłata pacjenta (od 0,01 zł do 452,70 zł).
- Dla 302 produktów ulegną obniżeniu ceny detaliczne brutto (od 0,01 zł do 69,65 zł).
- Dla 129 produktów wzrosną ceny detaliczne brutto (od 0,01 zł do 46,50 zł).
- W związku z wpłynięciem wniosków o skrócenie terminu obowiązywania decyzji refundacyjnych lub upłynięciem terminu obowiązywania decyzji refundacyjnych lub odmową refundacji na kolejny okres w obwieszczeniu nie znajdzie się 79 produktów bądź wskazań figurujących w poprzednim obwieszczeniu.
Źródło: Puls Medycyny




![Debata „Wyzwania na rok 2023 w polskiej medycynie” [WIDEO]](https://images.pb.pl/filtered/1e1b5ccb-9480-4eef-9a81-80a4426b86d9/cec53b65-30d6-5ffa-9e26-5c537431a514_xc_l.jpg)

![W Europie zanieczyszczenia powietrza powodują 800 tys. zgonów rocznie [WIDEO]](https://images.pb.pl/filtered/84b29d13-0727-4f42-8b21-de9566273376/76b0a951-3dc2-5503-975c-34480424e917_xc_l.jpg)
![Szansa na poprawę jakości życia dla pacjentów z HS [WIDEO]](https://images.pb.pl/filtered/08d54b79-36f0-499d-9e5e-731b6fdc1725/5e01a470-0cd4-51a2-9c4e-afeee2fc55b0_xc_l.png)