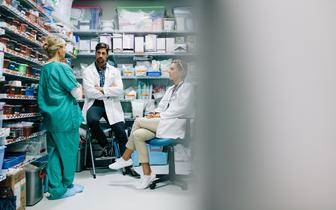
Branża farmaceutyczna odpowiada MZ ws. zaniżonych deklaracji dostaw leków: to efekt wadliwych przepisów DNUR
Jest odpowiedź branży farmaceutycznej na stwierdzenie Ministerstwa Zdrowia, że firmy wnioskując o kontynuację refundacji leków składają zaniżone deklaracje wielkości dostaw. - Sytuacja ta jest wynikiem wprowadzonych przez poprzedni rząd do ustawy refundacyjnej nieskonsultowanych z branżą farmaceutyczną wadliwych przepisów dotyczących kar za niezrealizowanie deklarowanej wartości dostaw leków - tłumaczy Krzysztof Kopeć, prezes PZPPF.

W czwartek (22 sierpnia) MZ wydało komunikat, z którego wynika, że firmy farmaceutyczne składając wnioski o objęcie refundacją i ustalenie ceny zbytu netto, zobowiązane są do zadeklarowania określonych wielkości dostaw. Jak sugeruje resort, deklaracje dotyczące wielkości dostaw leków refundowanych na przyszły rok są zaniżane.
MZ przypomniało, że w związku z pojawiającymi się problemami wynikającymi z interpretacji nowych zapisów ustawowych oraz realną możliwością ich wypełnienia w zakresie wielkości deklarowanych dostaw, minister zdrowia 12 kwietnia 2024 r. wydał stosowny komunikat w sprawie określenia deklarowanej wielkości dostaw, jednoznacznie określając wymagania, a także kryteria, jakie będą brane pod uwagę podczas każdorazowej weryfikacji poziomu wielkości dostaw we wnioskach refundacyjnych. Jak zaznaczono, Ministerstwo Zdrowia kierując się zasadą utrzymania dobrych relacji między stronami uczestniczącymi w procesach refundacyjnych, w przedstawionym stanowisku wyszło naprzeciw oczekiwaniom wielu interesariuszy wskazując na pewną elastyczność interpretacyjną w kontekście wzoru zawartego w art. 25 pkt 4 ustawy o refundacji leków.
W ocenie MZ, jednak część firm “korzyści płynące z partnerskiej postawy ” resortu część firm potraktowało jako przyzwolenie na przedkładanie deklaracji wielkości dostaw na nieracjonalnym poziomie pozbawionym jakiejkolwiek referencji do rzeczywistego zapotrzebowania na dany produkt. Co w efekcie prowadzi do nieprawidłowości identyfikowanych w ostatnim czasie w ramach trwających procesów refundacyjnych.
Resort zdrowia zaznaczył, że “dostrzegając negatywną tendencję firm farmaceutycznych w kontekście deklarowanych wielkości dostaw, dokonało kwerendy wniosków kontynuacyjnych o objęcie refundacją i ustalenie ceny zbytu netto na obwieszczenie Ministra Zdrowia w sprawie wykazu refundowanych leków na 1 stycznia 2025 roku, tzw. wielkie odnowienie”.
Ocena obejmowała prawie 1 600 wniosków, a jej zakres dotyczył deklarowanych wielkości dostaw proponowanych we wnioskach kontynuacyjnych na obwieszczenie refundacyjne obowiązujące od 1 stycznia 2025 r., w porównaniu z deklaracjami proponowanymi przez wnioskodawców we wnioskach obecnie obowiązujących decyzji refundacyjnych dla tych samych GTIN.
Jak zaznacza w komunikacie MZ, “wyniki dokonanej analizy danych jedynie utwierdzają co do kompletnego braku zrozumienia nadrzędnego celu zmian dotyczących deklarowanej wielkości dostaw zaimplementowanych Dużą Nowelizacją Ustawy o Refundacji, którym jest realne zapewnienie dostępności produktów zawartych na wykazie, o którym mowa w art. 37 ust. 1 ustawy o refundacji polskim pacjentom, ograniczając tym samym problemy związane z brakami leków na rynku.
Główne konkluzje ze wspomnianej powyżej analizy poziomu deklaracji dostaw dokonanej w stosunku do obecnie procedowanych wniosków kontynuacyjnych na 77 wykaz:
- Całkowita (łączna) liczba opakowań wszystkich leków w deklaracjach dostaw we wnioskach kontynuacyjnych na 1 stycznia 2025 r. vs wnioski z obecnie obowiązujących decyzji dla tych samych GTIN jest mniejsza aż o ponad 135 mln opakowań.
- 62% podmiotów odpowiedzialnych wykazało ujemny bilans deklarowanych wielkości dostaw całego portfolio produktów we wnioskach kontynuacyjnych na 1 stycznia 2025 r. vs wnioski z obecnie obowiązujących decyzji dla tych samych GTIN.
- Dodatni bilans deklarowanych wielkości dostaw całego portfolio produktów wykazało jedynie 38% podmiotów odpowiedzialnych w tożsamej sytuacji.
- Największa zidentyfikowana redukcja w deklaracji dostaw we wniosku kontynuacyjnym na 1 stycznia 2025 r. vs wniosek z obecnie obowiązującej decyzji dla tego samego GTIN wyniosła – 6 790 966 opakowań łącznie w I, II, i III rok refundacji – dotyczy produktu stosowanego w leczeniu nadciśnienia tętniczego.
W komunikacie podano zestawienie 20 podmiotów odpowiedzialnych, w stosunku co do których odnotowano największą sumaryczną różnicę deklarowanych dostaw we wnioskach kontynuacyjnych na 1 stycznia 2025 r. w stosunku do wniosków z obecnie obowiązujących decyzji dla tych samych GTIN.
W ocenie MZ szczególną niepewność oraz obawę wprowadzają postępowania podmiotów z dużą liczbą wniosków takich jak: Sandoz Polska Sp. z o.o., Teva Pharmaceuticals Polska Sp. z o.o. czy KRKA-POLSKA Sp. z o.o., które w swoim portfolio posiadają produkty o zróżnicowanym spektrum działania, niemniej największe redukcje w zakresie wielkości dostaw odnotowano w przypadku leków stosowanych w chorobach cywilizacyjnych (tj. leki hipotensyjne, leki kardiologiczne, leki hipolipemizujące, leki przeciwcukrzycowe) oraz antybiotyków. Te ostatnie stanowią grupę produktów o wysokim ryzyku potencjalnych problemów z dostępnością, czego Ministerstwo Zdrowia stale doświadcza w ostatnich latach. Z tego względu nieakceptowalnym jest modyfikowanie deklaracji dostaw redukując liczbę opakowań dostarczanych na rynek antybiotyków.
“Minister Zdrowia wyraża stanowczy brak akceptacji wobec deklaracji dalece odbiegających od faktycznych potrzeb polskich pacjentów, co będzie miało swoje odzwierciedlenie pod postacią negatywnych rozstrzygnięć na zaproponowanych warunkach. Brak jest racjonalnych powodów, dla których zasadnym byłoby umieszczanie na wykazie produktów, których producenci nie są w stanie zapewnić odpowiedniej dostępności, stwarzając wyłącznie mylne wrażenie pozornej dostępności refundacyjnej wywołując konsternację wśród pacjentów” - pisze MZ.
Dodaje: “Za naganną należy uznać postawę części podmiotów odpowiedzialnych wnoszących o modyfikację wniosków w zakresie deklarowanych wielkości dostaw na każdym z etapów procedowania, mając świadomość implikacji takiego postępowania oraz konieczności każdorazowego rozstrzygnięcia przedmiotowej kwestii przez Ministra Zdrowia co sprowadza do ingerencji decyzyjnej kilkukrotnie w ciągu całego postępowania. Należy również podkreślić, że dla pozostałych elementów wniosku refundacyjnego zmiany są wnoszone incydentalnie. Wskazane praktyki, w świetle trwających prac nad mającym miejsce cyklicznie co trzy lata wielkim odnowieniem decyzji refundacyjnych, w opinii Ministra Zdrowia należałoby traktować jako niezrozumiałe utrudnianie toczących się postępowań administracyjnych.
Producenci leków: to efekt nieskonsultowanych zmian w ustawie refundacyjnej
O komentarz “Puls Medycyny” poprosił prezesa Polskiego Związku Pracodawców Przemysłu Farmaceutycznego – Krajowi Producenci Leków Krzysztofa Kopcia. - Sytuacja ta jest wynikiem wprowadzonych przez poprzedni rząd do ustawy refundacyjnej nieskonsultowanych z branżą farmaceutyczną wadliwych przepisów dotyczących kar za niezrealizowanie deklarowanej wartości dostaw leków. Kary mają być nakładane na producenta nawet wówczas, gdy leków na rynku nie zabraknie, a ich szokująca wysokość jest niczym nieuzasadniona. W efekcie firmy w obawie przed karą za niedostarczenie leków z przyczyn niezależnych od nich zaniżyły wielkość deklarowanych dostaw, wcale nie mając zamiaru ich zmniejszać. Aby tę sytuację rozwiązać, wszystkie organizacje zrzeszające producentów leków zwróciły się z prośbą do resortu zdrowia, aby zorganizować spotkanie, na którym zostaną wypracowane najlepsze dla pacjentów i bezpieczne dla firm rozwiązania - wskazuje Kopeć.
Przypomnijmy, że MZ przedstawiło już propozycję zmian w ustawie o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (tzw. ustawa refundacyjna). To tzw. szybka nowelizacja ustawy refundacyjnej (SZNUR).
Zmiany mają usprawnić proces refundacyjny, a dzięki temu dostępność leków ma się poprawić.
Źródło: Puls Farmacji


![Prof. Ciach: nasze odkrycie przedłuży przydatność organów do przeszczepu, może poprawić ich jakość [WYWIAD]](https://images.pb.pl/filtered/e26c445a-5e1b-4a03-b026-86ef81f90d39/6f800abc-080d-54b1-bf1c-8c0ae82805a0_xc_l.jpg)

![W Europie zanieczyszczenia powietrza powodują 800 tys. zgonów rocznie [WIDEO]](https://images.pb.pl/filtered/84b29d13-0727-4f42-8b21-de9566273376/76b0a951-3dc2-5503-975c-34480424e917_xc_l.jpg)
![Szansa na poprawę jakości życia dla pacjentów z HS [WIDEO]](https://images.pb.pl/filtered/08d54b79-36f0-499d-9e5e-731b6fdc1725/5e01a470-0cd4-51a2-9c4e-afeee2fc55b0_xc_l.png)